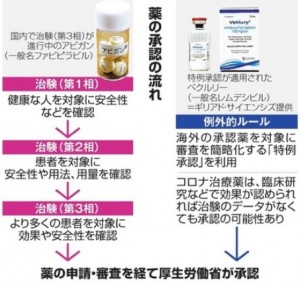
薬の開発には、効果や安全性を確かめるための臨床試験に時間と手間がかかります。動物実験などの基礎研究を除くと、一般に三つの段階を踏んで進められます。まず少人数の健康な人に使ってもらって、体に害がないかを確かめる第1相、最適な使い方や量を探る第2相、最終的に効果の裏付けをする第3相まであります。ひとつの新薬を開発するだけでも数年~十数年という長い時間と、500億~1千億円といった巨額のお金がかかると言われています。
新型コロナの治療薬やワクチンの開発にもやはり時間がかかっています。ベクルリー(一般名レムデシビル)という薬は、新型コロナへの対応を急ぐため、特例承認という制度を使っています。海外で販売を認められた薬について、海外での臨床試験のデータをもとに国内で使えるようにする仕組みを利用しています。アビガン(一般名ファビピラビル)は、もともと新型インフルエンザの薬でしたが、厚生労働省は、特例で国内の審査を簡略化して今年5月中の承認を目指しましたが、十分なデータが集まらず、まだ認められていません。
(2020年6月26日 朝日新聞)
(吉村 やすのり)