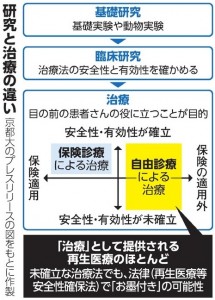
国内で治療として提供される再生医療のなかに、国際学会が非難するような治療法や、科学的に確立していない治療法が多数含まれています。京都大学の研究チームは、2,377の医療機関が提供する3,467件の再生医療の安全性と有効性を分析しています。培養した幹細胞を投与する治療法では、筋肉や骨などの疾患や美容整形を目的としたものが多く、科学的根拠が十分ではないがん免疫療法も多数確認されました。
日本では、2014年から運用される再生医療等安全性確保法にもとづいて、再生医療を提供する医療機関は計画をつくり、第三者の再生医療等委員会の審査を受ける必要があります。しかし、再生医療の安全性・有効性は、日常的な診療の一環として提供できるほど厳密に証明されてはいないことが指摘されています。わが国では、このような治療に再生医療等委員会の承認というお墨付きが与えられている可能性が否定できないとしています。
厚生労働省研究班の報告によれば、専門外の医師が再生医療を提供している可能性があること、安全性にかかわる研究論文の引用が計画書にないことなどが指摘されています。これまでの研究と治療の分類を見直し、治療の中でも未確立な技術を使ったものは、未確立医療と位置づけを明確にすることを提案しています。
患者が再生医療を受けたいと考えた時、どんな標準治療や研究への参加など他の選択肢はないかを検討したり、再生医療を受ける場合には費用が明示されているかどうかを確認することが大切です。特に、患者の体験談や、同じ細胞が様々な疾患に効く、リスクがないという主張は要注意です。また、ウェブサイトなどで再生医療法にのっとっていますなどの特別な許可を得たかのように強調することは、医療広告の規制で禁止される誇大広告にあたる可能性があります。
(2022年10月26日 朝日新聞)
(吉村 やすのり)