新型コロナウイルス感染症の治療薬として期待が高まるアビガンの国内での早期承認が注目されています。厚生労働省は、申請後の審査の期間を短縮して年内の承認を目指していますが、緊急的な対応での特例扱いでどこまで早められるかは未知数です。米欧などに比べ、薬を現場で使えるようにするまでの仕組みが硬直的で、スピード感が劣ります。薬が患者に使えるようになるまでには、大きく2つの段階があります。安全性や有効性を臨床試験で確かめる治験と、製薬会社の申請を受けて治験の結果を検証・評価する承認審査です。
アビガンは、富士フイルム富山化学が抗インフルエンザウイルス薬として2014年に製造・販売の承認を得ています。新型インフルエンザの流行を念頭にした備蓄用で、一般に流通はしていません。今の備蓄は200万人分あります。新型コロナでは、1人の治療にインフルの3倍の量が必要とされ、コロナ患者では約70万人分に相当します。
インフル薬として承認済みのアビガンも、新型コロナでは投与量が3倍と大幅に異なるため、安全性などを改めて確かめる必要があります。6月末までに順調に治験が終われば申請手続きに入ります。日本では、通常承認審査に1年かかります。厚生労働省が早期の承認に慎重な背景には、1970~1980年代の薬害エイズ事件の苦い記憶があります。アビガンは胎児に奇形が生じる可能性が指摘されており、副作用への目配りが必要となります。
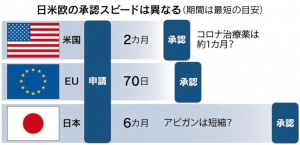
米欧はスピード感と柔軟性があります。米国は国家の安全に重大な影響がある緊急時は、米食品医薬品局(FAD)が未承認の医薬品でも使用を認める仕組みがあります。EUでも、医薬品を審査する欧州医薬品庁(EMA)も緊急承認の手続きがあります。通常約210日の承認審査を約70日にする制度です。安全性をs重視する日本と、スピード感を重視する欧米との違いが出ています。
(2020年4月27日 日本経済新聞)
(吉村 やすのり)