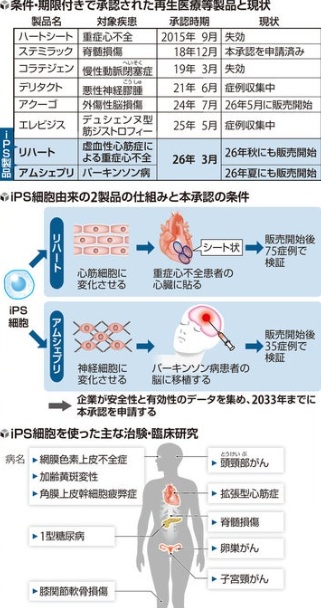
iPS細胞から作った2つの再生医療等製品が、3月に条件・期限付きで承認されました。2製品は、大阪大学発新興企業クオリプスが開発したリハートと、製薬大手・住友ファーマが手がけたアムシェプリです。リハートは虚血性心筋症による重症心不全が対象で、シート状の細胞を患者の心臓に貼ります。アムシェプリは神経難病のパーキンソン病が対象で、患者の脳に移植します。
2製品は数か月以内に国の審議を経て、公的医療保険の適用の有無と価格が決まり、販売開始となります。iPS製品の実用化は、患者が待望した成果と言えます。しかし治験の参加者はリハートで8人、アムシェプリで7人と少ないため、早期承認の対象となり、製品の有効性の判定は推定にとどまっています。
早期承認は、再生医療や遺伝子治療の薬など再生医療等製品を対象に、自動車免許で言えば仮免許を与える制度です。2014年11月に導入され、有効期間は原則7年以内です。この間に申請企業は症例を集め、本承認を再申請する必要があります。有効な症例が集まらなければ、承認は失効します。これまで8製品が早期承認を得ましたが、施行から約11年で本承認はゼロです。実用化しても、広く普及する保証はありません。
企業が再生医療等製品の開発費を回収するには、高価でなければ事業が成り立ちません。早期承認で公的医療保険が適用されると、製品は原則患者の3割負担となります。価格が高くても高額療養費制度の適用を受ければ、患者負担は多くても月数十万円程度で済みます。患者は新製品を利用しやすく、企業が高価な製品を開発する意欲につながりますが、医療保険財政を圧迫することになります。
科学誌Natureは、日本の早期承認制度に疑問を呈しています。医薬品の有効性や安全性の確認には大規模な治験が必要で、早期承認は、開発の経済・倫理的コストを患者や納税者、保険会社に押しつけることになります。iPS細胞の研究は大切ですが、開発を急いで安全性を軽視してはいけません。
(2026年4月1日 読売新聞)
(吉村 やすのり)






